「ジェネリック医薬品」と
「バイオ後続品(バイオシミラー)」の活用
「ジェネリック医薬品」と
「バイオ後続品(バイオシミラー)」とは
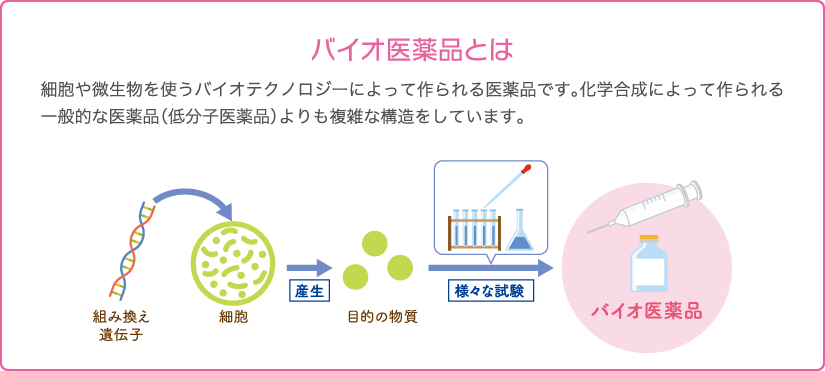
新薬の特許が切れてから別の会社で発売される同じ成分の医薬品を後発薬といいます。後発薬には化学合成品の後発薬「ジェネリック医薬品」と生物の力を利用して作るバイオ医薬品の後発薬である「バイオ後続品(バイオシミラー)」の2種類があります。いずれも薬価(薬の価格)が安くなっています。

バイオ後続品(バイオシミラー)とは
近年登場したバイオ後続品(バイオシミラー)をご存知でしょうか。
今まで飲み薬などジェネリック医薬品が作られているようなお薬は、化学合成で作られる分子量が小さい医薬品が中心でした。科学技術の発展でバイオ医薬品と呼ばれる、遺伝子組み換え技術や細胞培養技術などのバイオテクノロジーによって作られる分子量の大きい医薬品が登場し、がんや関節リウマチなどの病気で治療法が飛躍的に進歩しました。
バイオ後続品(バイオシミラー)とは、既に発売しているバイオ医薬品(先行バイオ医薬品)と品質や有効性、安全性が同等・同質*と認められたバイオ医薬品です。バイオ後続品(バイオシミラー)は、厳密な管理の中で製造され、多くの試験を経て、効果と安全性が同等・同質であることを証明するために実際の患者さんを対象とした臨床試験を行っています。そして、先行バイオ医薬品と同等・同質であると認められたものが、お薬として使われています。
バイオ後続品(バイオシミラー)は、構造が複雑なタンパク質でできており、先行バイオ医薬品と全く同じ薬が製造できないため、シミラーという表現を使います。そのためジェネリック医薬品よりも多くの品質試験が必要とされ、最終的に臨床試験を行って同等・同質であることを確認しています。ジェネリック医薬品とは認可の基準が異なるため別の呼び方をします。
バイオ後続品(バイオシミラー)の薬価は、先⾏バイオ医薬品の約7割になるように定められています。
*同等・同質:品質の類似性が高く、品質に何らかの差異があっても安全性・有効性に影響を及ぼさないこと。
バイオ後続品(バイオシミラー)はなぜ安いのでしょうか
⼀般的に新薬(先行バイオ医薬品)の研究開発には、10〜20年程度もの⻑い年⽉と多額の費⽤が必要であるといわれており、研究開発にかかったコストがお薬の価格に反映され、「薬価」として⽇本全国どこの医療機関でも同じ価格に定められています。
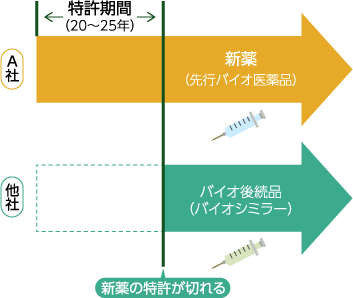
また、先行バイオ医薬品には独占的に販売できる期間が定められています。それが「特許期間」で、新薬の研究開発から20〜25年間は、他の医薬品メーカーはバイオ後続品(バイオシミラー)を製造することはできません。
この特許期間が終わると、新薬の成分は国⺠共有の財産となるため、ようやく他の医薬品メーカーがバイオ後続品(バイオシミラー)として製造・販売できるようになります。
バイオ後続品(バイオシミラー)を製造する際には、一般的に開発などに要する時間や費⽤が少なく、コストを抑えることができます。

※自己負担額が高くなりすぎないようにする仕組み(高額療養費制度)との関係で、バイオ後続品(バイオシミラー)を使っても、自己負担額が必ずしも下がらない場合もあります。
「有効性と安全性が同等・同質」と認められています
バイオ後続品(バイオシミラー)は先行バイオ医薬品と同じように、国で定められた法律*に基づいて厚⽣労働⼤⾂の承認を得ています。バイオ後続品(バイオシミラー)は品質などを確認するさまざまな試験に加え、一般的に大規模な臨床試験(治験)を行うことで、先行バイオ医薬品と同等・同質の品質と有効性、安全性を有しているかを確認します。
これらの試験の結果、国で定められた基準をクリアしたものがバイオ後続品(バイオシミラー)として承認されています。「有効性、安全性が先行バイオ医薬品と同等・同質である」と認められたお薬ですから、先行バイオ医薬品と同じように使⽤することができます。
*医薬品、医療機器等の品質、有効性及び安全性の確保に関する法律(薬機法)


※ただし、先行バイオ医薬品が複数の効能・効果を持っている場合は、バイオシミラーがその全ての効能・効果を持っているわけではないことがあります。
参考:バイオ医薬品・バイオシミラーを正しく理解していただくために(患者・一般の方向け)平成31年2月版(厚生労働省)https://www.mhlw.go.jp/content/10800000/000496082.pdf(2025年6月参照)
監修者略歴
日本臨床腫瘍薬学会(JASPO)顧問
遠藤 一司(えんどう かずし)先生
- 【学歴・職歴等】
昭和48年明治薬科大学製薬学科卒業
厚生省(現厚生労働省)監視指導課薬事専門官、医療課医療指導監査官、
老人保健課課長補佐、北海道地方医務局薬事専門官
厚生労働省薬事・食品衛生審議会 臨時委員(医薬品安全対策調査会担当)
医薬品基金(現医薬品医療機器総合機構)調査役、企画課長
北海道がんセンター・国立がんセンター東病院薬剤部長
明治薬科大学医薬品安全管理学 教授
明治薬科大学 客員教授・評議員
日本病院薬剤師会 副会長・専務理事
日本臨床腫瘍薬学会 理事長
- 【現在】
日本臨床腫瘍薬学会(JASPO) 顧問
北海道薬剤師会 副会長
厚生労働省サリドマイド及びレナリドミドの安全管理に関する検討会 構成員
RevMate第三者評価委員会 委員
日本薬学図書館協議会 理事
日本薬剤師研修センター 特別顧問
日本病院薬剤師会 名誉会員



